ТРИАРИЛМЕТИЛЬНЫЕ РАДИКАЛЫ
,
Аr3С. Многие Т. р. существуют в равновесии с димерами,
нек-рые выделены в индивидуальном состоянии. Строение димера зависит от природы
Т. р. Трифенилметил (С6Н5)3С• образует
димер циклогексадиенового строения:
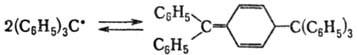
Нек-рые Т. р. димеризуются
в гексаарилэтаны: 2Аr3С 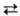 Аr3С—САr3. Наиболее устойчивы перхлорирован-ные Т. р.
(С6Сl5)3С•, разлагающиеся лишь при
нагр. до 300 °С.
Аr3С—САr3. Наиболее устойчивы перхлорирован-ные Т. р.
(С6Сl5)3С•, разлагающиеся лишь при
нагр. до 300 °С.
Неспаренный электрон в
Т. р. делокализован по системе p-связей, более 50% спиновой плотности сосредоточено
на центр. атоме С. Т. р. поглощают в области 200-400 нм (e ~ 104)
и 500-650 нм (e 102-103).
Т. р. (за исключением перхлорированных)
легко реагируют с О2, NO, NO2, активными своб. радикалами;
восстанавливаются в соответствующие углеводороды; со щелочными металлами образуют
соли; с галогенами - три-арилметилгалогениды.
Получают Т. р. восстановлением
триарилметилгалоге-нидов (или перхлоратов), восстановлением триарилме-тилкарбкатионов
и окислением триарилметилкарбанио-нов, напр.:
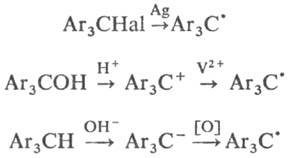
По св-вам к Т. р. близки
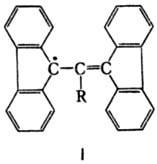
замещенные аллильные радикалы, напр. бис-(бифенилен)аллилы (ф-ла I; R
= Н, СН3, Аr).
Первый Т. р.-трифениметил
получил М. Гомберг в 1900. См. также Радикалы свободные
.
Лит.: Розанцев Э.
Г., Шолле В. Д., Органическая химия свободных радикалов, М., 1979, с. 99-128.
В. Д. Шолле.
|

