|
Реклама |
|
|
 |
* Т-ра разложения. Полимерные сопряженные
П. обладают большой тепло- и термостойкостью (напр., В спектрах ИК и комбинац.
рассеяния П. присутствует характеристич. полоса при 2100-2200 см -1. Тройные связи в П. способны
к р-циям присоединения и изомеризации. Олигомерные сопряженные П. вступают в
р-ции нуклеоф. присоединения легче, чем ацетилен. Так, они легко присоединяют
HCN, тогда как ацетилен - только в присут. катализаторов. При электроф. присоединении
реакц. способность таких П. быстро падает с увеличением числа связей С Сопряженные циклич. и линейные
П. способны к твердофаз-ной топохим. полимеризации, при к-рой почти не меняется
кристаллич. структура. В несопряженных П. связи
С Получают П. окислит. димеризацией
соответствующих ацетиленовых производных через их медные соли (р-ция Г лазера,
ур-ние 1); по Кадио - Ходкевича реакции
(2); де-гидрогалогенированием
1,1- или 1,2-дигалогенидов (3): По р-ции Глазера из ацетилена
получают Для синтеза полимерных
П. (в т.ч. содержащих связи С Циклические П. используют
для синтеза аннуленов. He-к-рые П. проявляют бактерицидные св-ва. Лит.: Сладков A.
M., Кудрявцев Ю. П., "Успехи химии", 1963, т. 32, в. 5, с. 509-38;
Прогресс полимерной химии. Сборник, под. ред. В. В. Коршака, M., 1969, с. 87-102;
Шостаковский M. Ф., Богданова А. В., Химия диацети-лена, M., 1971; Станкевич
И. В., Томилин О. Б., "Ж. структурной химии", 1977, т. 18, №4, с.
772-73; Мисин В. M., Черкашин В. M., "Успехи химии", 1985, т. 54,
в. 6, с. 956; Коршак В. В. [и др.], "Доклады АН СССР", 1988, т.
300, № 4, с. 889-892. Ю. П. Кудрявцев. |

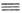 С.
С. C)5
CH=CH2, CH3CH=CH(C
C)5
CH=CH2, CH3CH=CH(C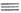 C)4CH=CH2.
В микроорганизмах найдены полииновые антибиотики: биформин H(C
C)4CH=CH2.
В микроорганизмах найдены полииновые антибиотики: биформин H(C C)3—
-CH2CH(OH)CH2OH и агроцибин H(C
C)3—
-CH2CH(OH)CH2OH и агроцибин H(C C)3CH=
=СНСН2ОН. К природным П. относят также карбин, аллотропную форму
углерода.
C)3CH=
=СНСН2ОН. К природным П. относят также карбин, аллотропную форму
углерода.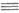 C)4H
разлагается при обычных условиях. Олигомерные П. чувствительны к свету. Их устойчивость
увеличивается при замещении концевых водородных атомов алкильными или арильными
заместителями (т-ры плавления таких соед. приведены в табл.).
C)4H
разлагается при обычных условиях. Олигомерные П. чувствительны к свету. Их устойчивость
увеличивается при замещении концевых водородных атомов алкильными или арильными
заместителями (т-ры плавления таких соед. приведены в табл.).
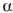 -карбин
переходит в графит при 2300 0C, не разлагаясь), а также фотоэлектрич.
чувствительностью.
-карбин
переходит в графит при 2300 0C, не разлагаясь), а также фотоэлектрич.
чувствительностью. С.
Восстановление полииновых спиртов приводит к кумуленам, напр.:
С.
Восстановление полииновых спиртов приводит к кумуленам, напр.: 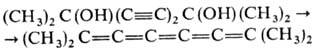
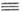 С обладают
одинаковой реакц. способностью и независимы друг от друга.
С обладают
одинаковой реакц. способностью и независимы друг от друга.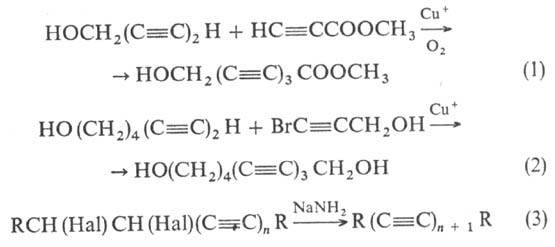
 -карбин.
-карбин. C
в боковых цепях) используют р-ции поликонденсации (4), селективной полимеризации
разл. мономеров по связям С
C
в боковых цепях) используют р-ции поликонденсации (4), селективной полимеризации
разл. мономеров по связям С С
(5) или C=C (6):
С
(5) или C=C (6):